瀰漫性大B細胞淋巴瘤的基因分型 Molecular Genetic Classification of DLBCL:流變與細項
此為 2026 年 3 月 fellow book reading 第二部份
在上一篇文章的最後,我們提到了基因型也可以作為使用特定標靶藥物的參考。
基因分型拆解 DLBCL 的流變
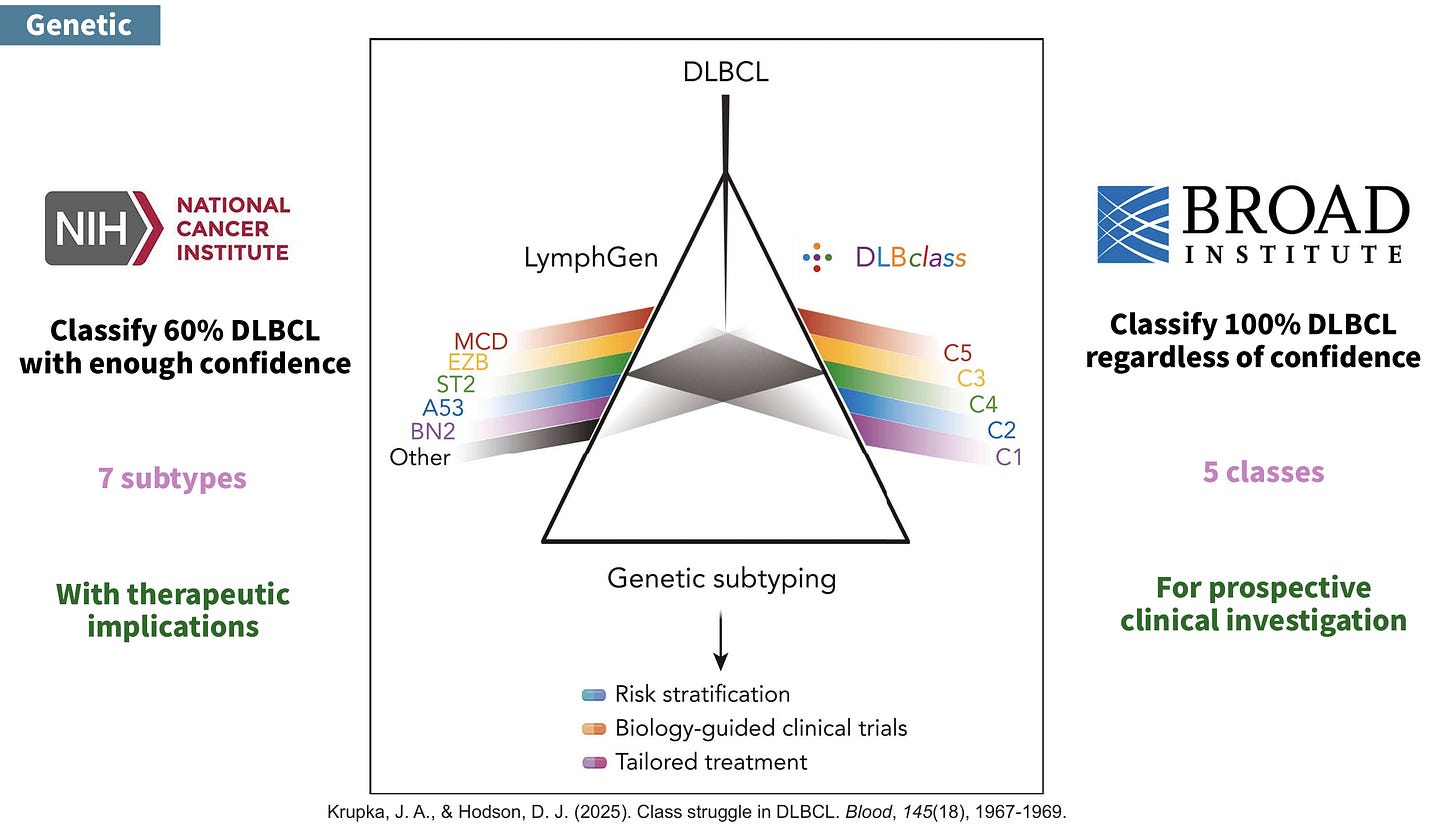
目前最常被使用的基因分型系統是 NCI 發展出來的 LymphGen,再來便是 Broad Institute 研發出來一個很類似的 DLBclass。
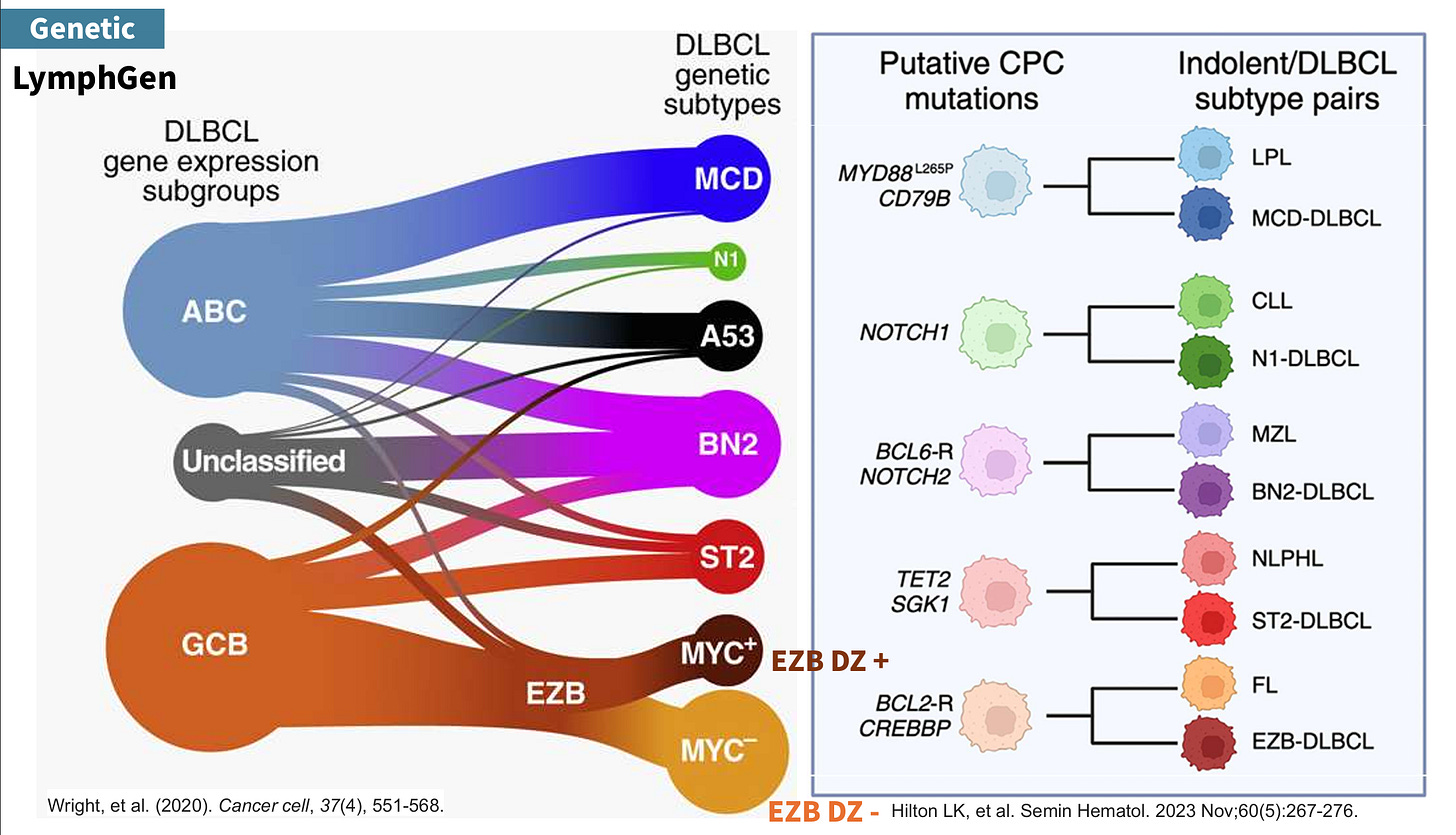
LymphGen 前身為 GenClass (Roland Schmitz, George W. Wright, Ph.D…etc al, NEJM, 2018),區分出 MCD, BN2, N1, EZB,兩年後發表了 LymphGen (George W. Wright & Louis M. Staudt, Cancer Cell, 2020),再細分出 EZB 的 MYC +/-,再加上 ST2 與 A53。從 GenClass 到 LymphGen 的改進,可以把先前無法被分類的(unclassifiable)54% 給分完。然而,還是剩了大約 40% 的 DLBCL, NOS 無法有個對應的基因分型。
在 LymphGen 發表之後,有幾個驗證的研究也相繼發表:
紀念斯隆-凱特琳癌症中心(Memorial Sloan Kettering Cancer Center, MSKCC)以快要四百名個案進行驗證 (Meng-Lei Zhu, Letter in Haematologica, 2024),發現 LymphGen 只能將 55% 的個案進行分類。
英國血液腫瘤研究網絡(Haematological Malignancy Research Network, HMRN)用九百多名個案進行驗證,也只能給予 53% 名病人進行分型 (Hendrik F P Runge from Cambridge, Br J Haematol, 2021)。
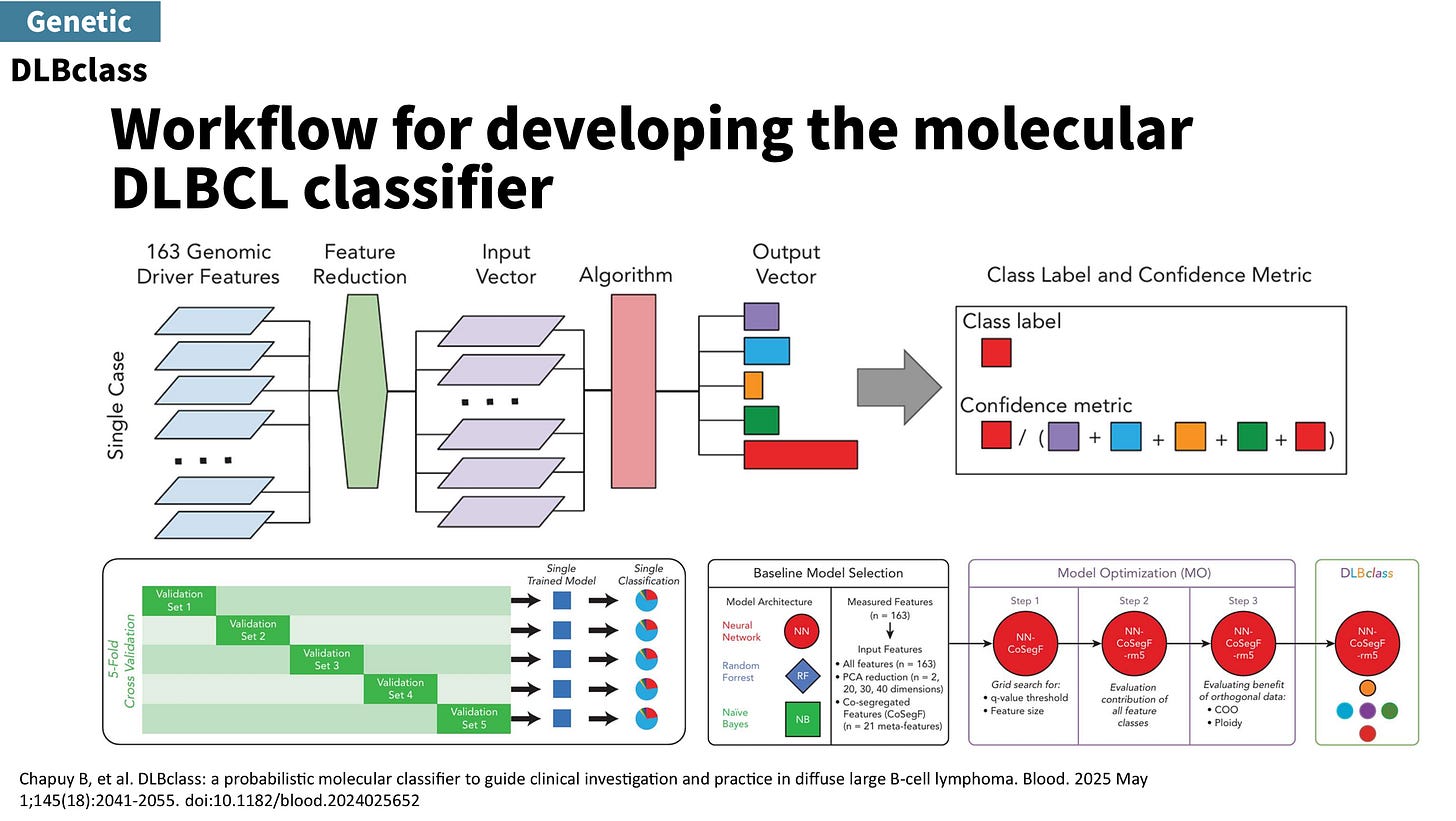
位在生醫矽谷波士頓的龍頭麻省理工-哈佛布洛德研究所(Broad Institute of MIT and Harvard)也出手希望用強大算力破解 DLBCL (Chapuy, Nature medicine, 2018),並在 2025 年正式發表 DLBclass (Chapuy, Blood, 2025)。有別於 LymphGen 以貝氏定理(probabilistic bayesian)為核心,DLBclass 的核心則是機器學習,並納入了神經網路(neural network)、隨機樹(random forest),與貝氏分類器(naive Bayes classifier)。為了處理 LymphGen 無法分型的問題,DLBclass 會確保每個個案都有個分類,但也因此被詬病它的分類無視信心程度,會有準確度的問題。簡單來說就是硬把每個個案塞到籃子裡。
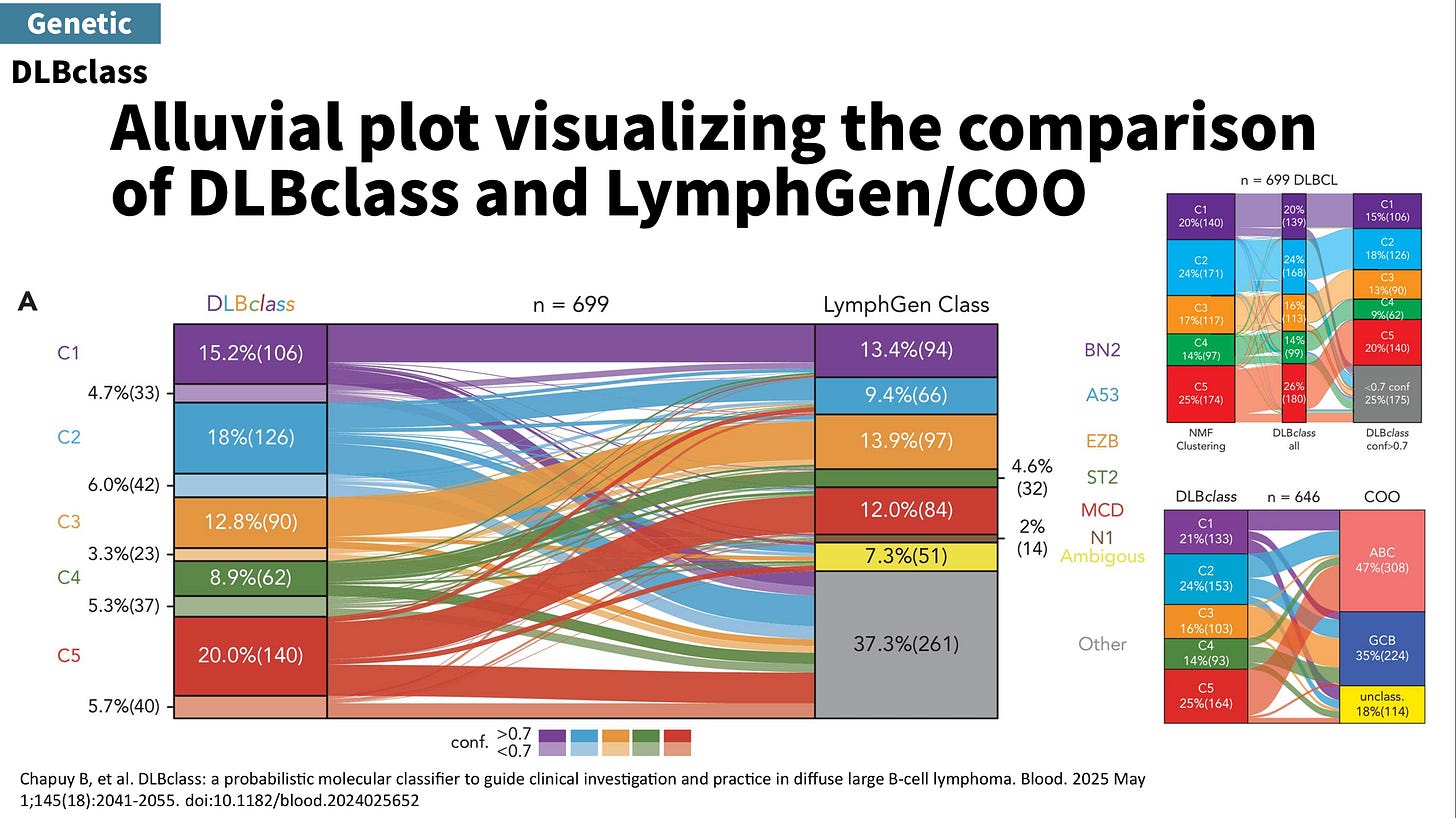
LymphGen 分出了七類,不過 DLBclass 只有五類。N1 與 double-hit–like (EZB-MYC) 在 DLBclass 並不是獨立的 subtype。
同個個案用不同系統來分型的話則用沖積圖(Alluvial plot)來表示。
DLBCL 有哪些基因分型:以 LymphGen 為主架構
DLBCL 的形成除了新生的(do novo)以外,還有從比較低惡性度淋巴瘤(indolent lymphoma)轉變而來的可能。LymphGen 則發現這些基因分型大部份能找到相對應的低惡性度淋巴瘤:MCD 型對應至淋巴漿細胞淋巴瘤(Lymphoplasmocytic lymphoma, LPL)、N1 型對應至慢性淋巴性白血病 (chronic lymphocytic leukemia, CLL) / 小淋巴細胞淋巴瘤 (Small Lymphocytic Lymphoma, SLL)、BN2 對應到邊緣區淋巴瘤(Marginal Zone Lymphoma, MZL)、ST2 型至結節性淋巴球為主型的何杰金氏淋巴瘤 (Nodular Lymphocyte-Predominant Hodgkin Lymphoma, NLPHL),以及 EZB 型至濾泡性淋巴瘤 (Follicular Lymphoma, FL)。
細部的分型如下:
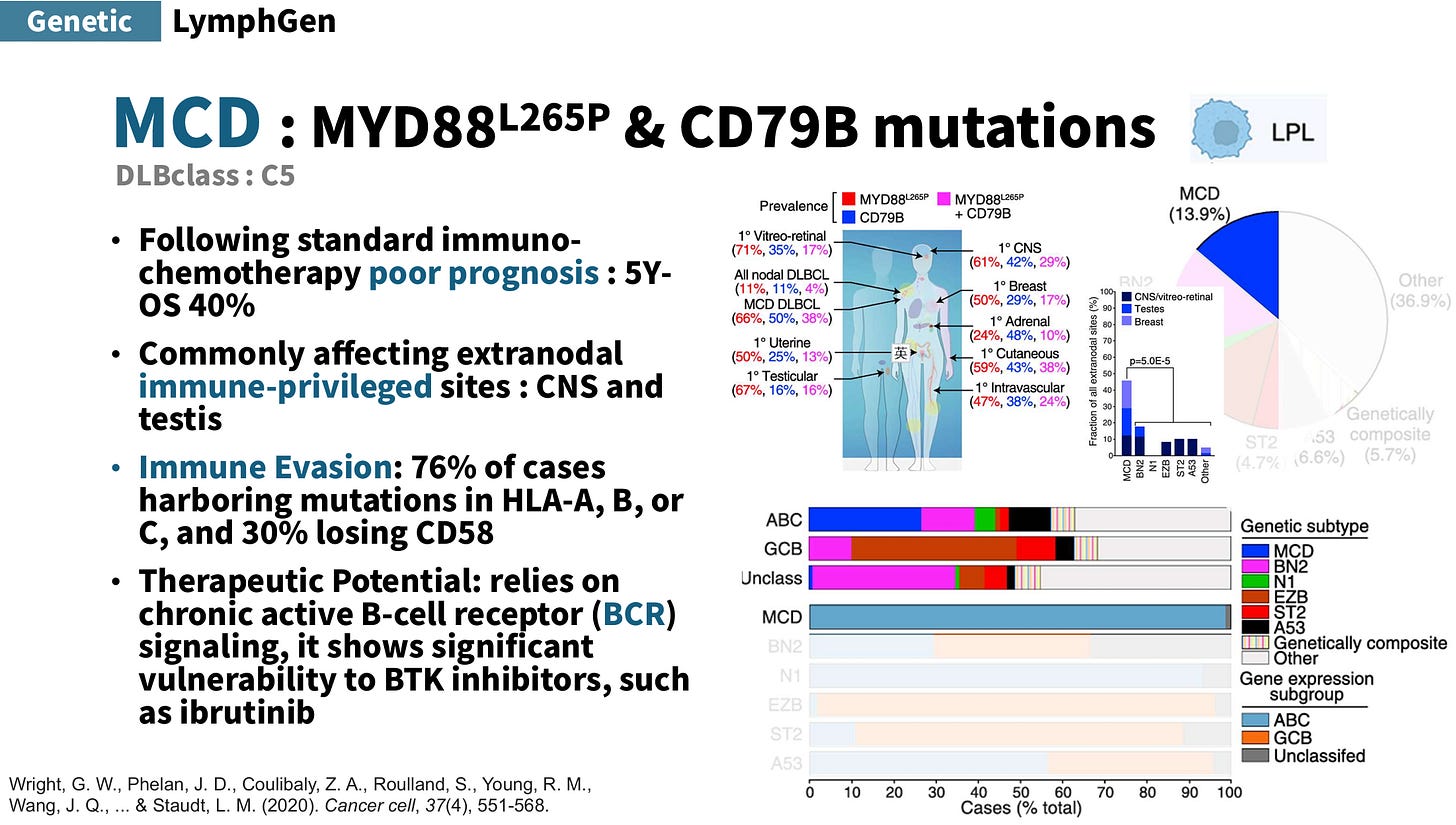
MCD 型/DLBclass-C5:以 MYD88L265P & CD79B 突變為主,接受標準免疫化療的預後差,5 年 OS 約 40%。常侵犯免疫特權的結外部位,尤其是中樞神經與睪丸。具免疫逃脫(immune evasion)特性,約 76% 病例帶有 HLA-A/B/C 突變、30% 有 CD58 缺失。因機轉上依賴慢性活化的 BCR signaling,對 BTK inhibitors (e.g., ibrutinib) 有顯著脆弱性。
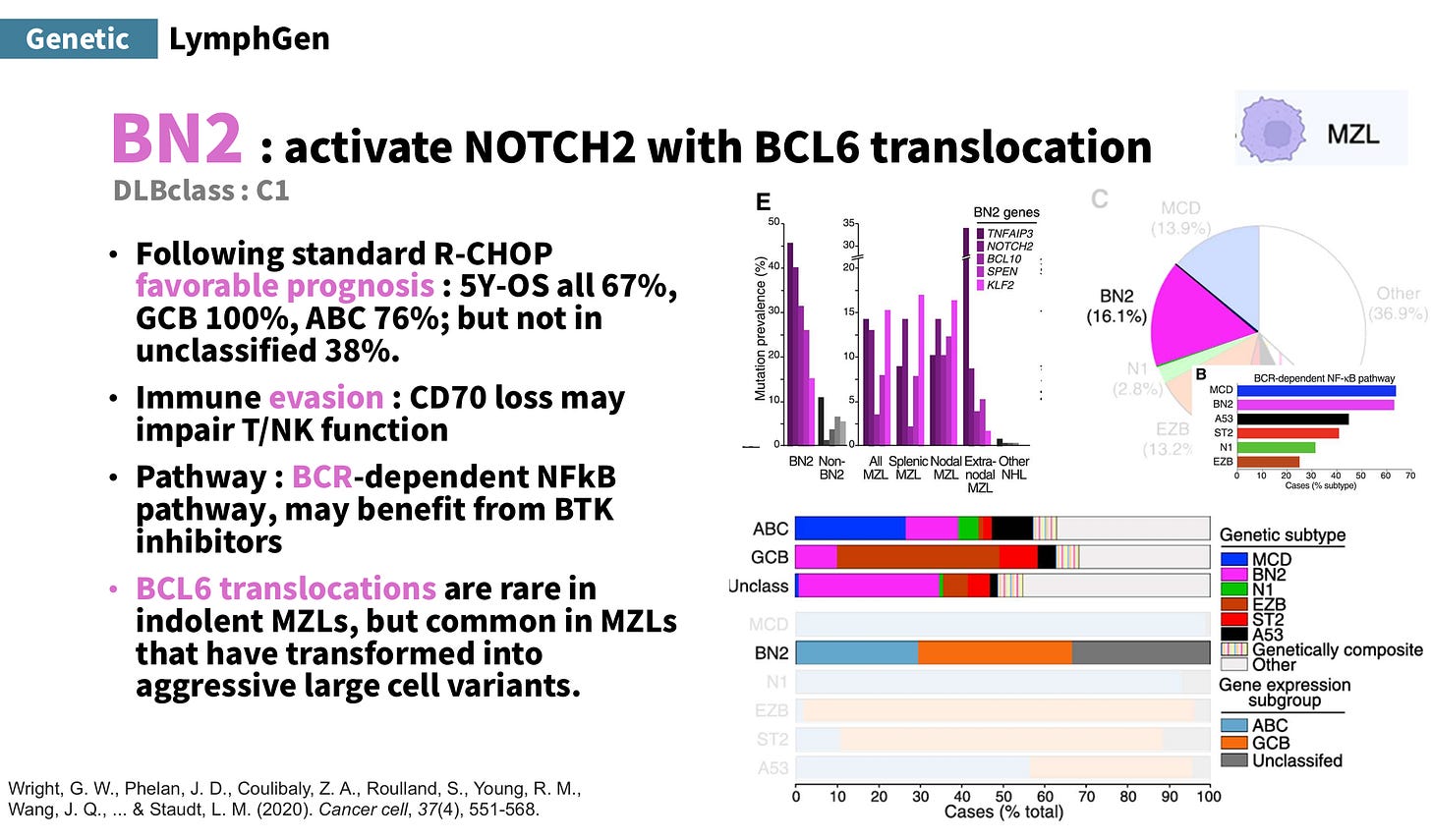
BN2 型/DLBclass-C1:代表基因特徵為 NOTCH2 活化 + BCL6 translocation。接受標準 R-CHOP 後,整體屬較佳預後,5 年 OS 約 67% (GCB 100%, ABC 76%),但 unclassified 僅 38%。和 MCD 同樣具免疫逃脫特性,但機轉上則是 CD70 loss 可能損害 T/NK cell 功能。訊號路徑也以 BCR-dependent NF-κB pathway 為主,因此也可能受益於 BTK inhibitors。另外 BCL6 translocation 在 MZL 少見,但在轉化成侵襲性大細胞變異型的 MZL 中較常見。
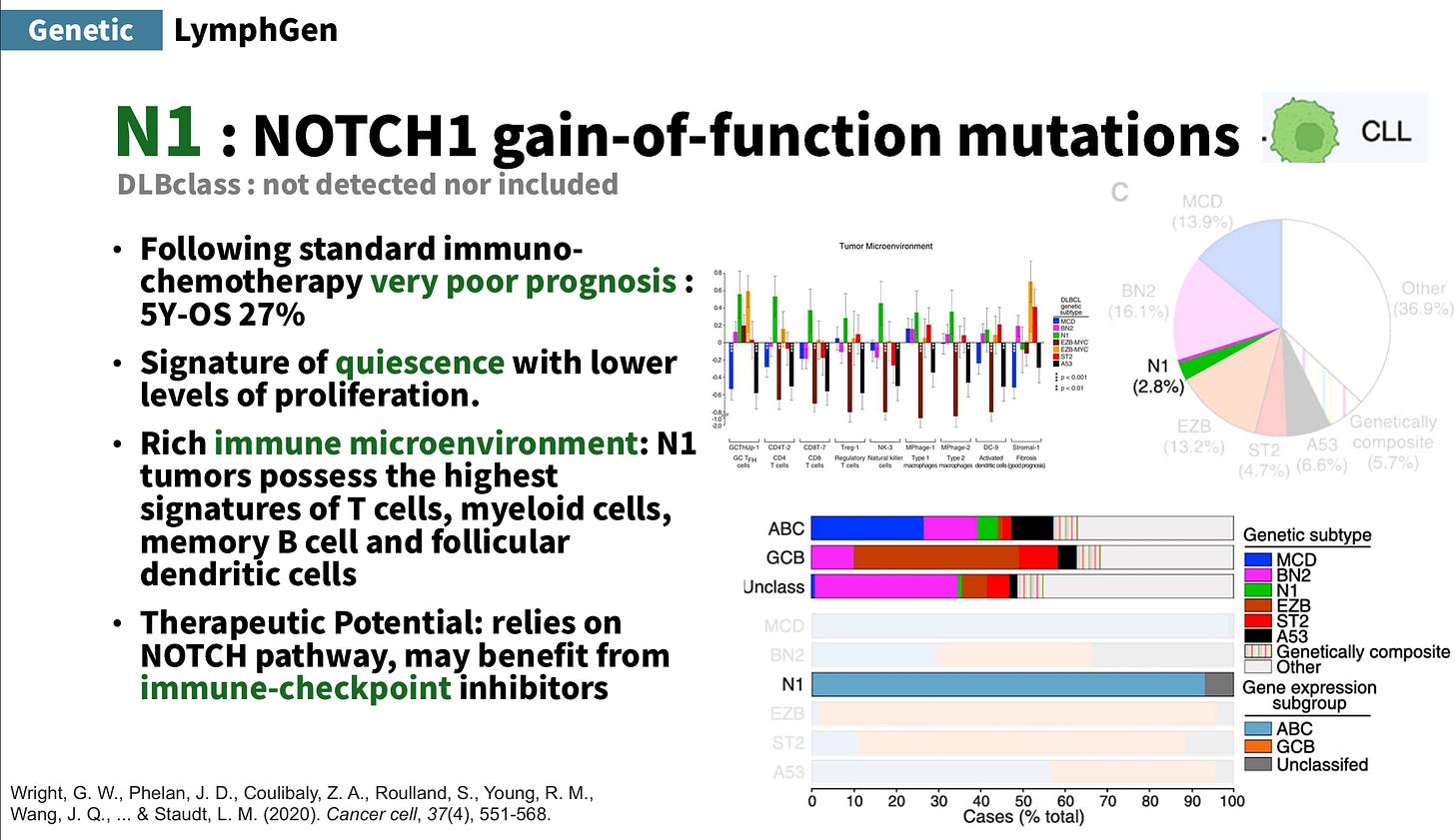
N1 型/DLBclass未納入:代表基因特徵為 NOTCH1 gain-of-function 突變,接受標準免疫化療後,預後很差,5 年 OS 約 27%。生物學特徵呈現 quiescence signature,即增殖較低,而腫瘤微環境則具有豐富 immune microenvironment
T cells, myeloid cells, memory B cells, follicular dendritic cells,可能受益於 immune-checkpoint inhibitors。
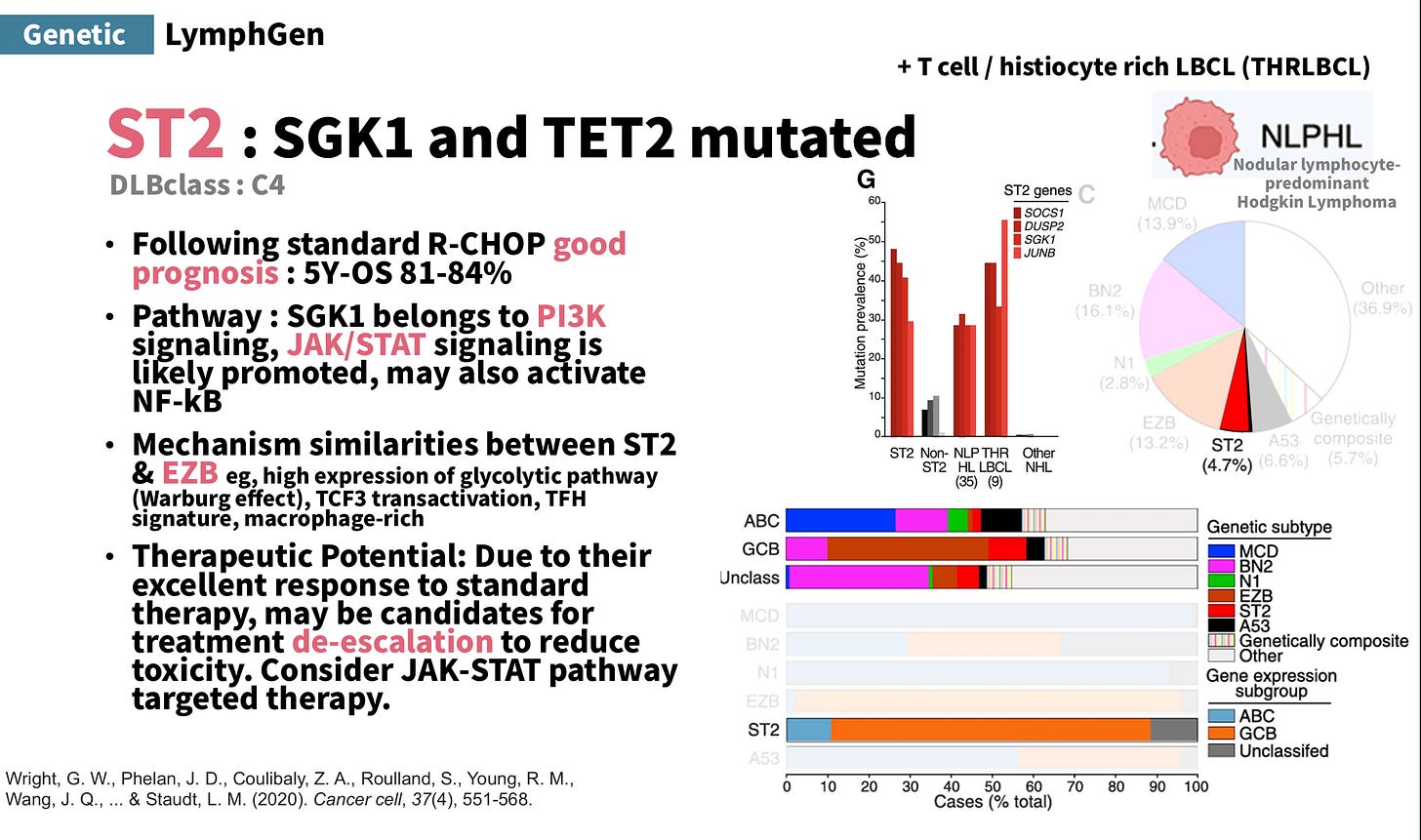
ST2 型/DLBclass-C4:代表基因特徵為 SGK1 與 TET2 突變。接受標準 R-CHOP 後,屬良好預後,5 年 OS 約 81–84%。SGK1 屬於 PI3K signaling、JAK/STAT signaling 可能被促進,也可能活化 NF-κB,具時具有高表現糖解代謝路徑(Warburg effect)。因對標準治療反應佳,可考慮降階治療(de-escalation)以減少毒性
也可考慮 JAK-STAT pathway 的標靶治療。
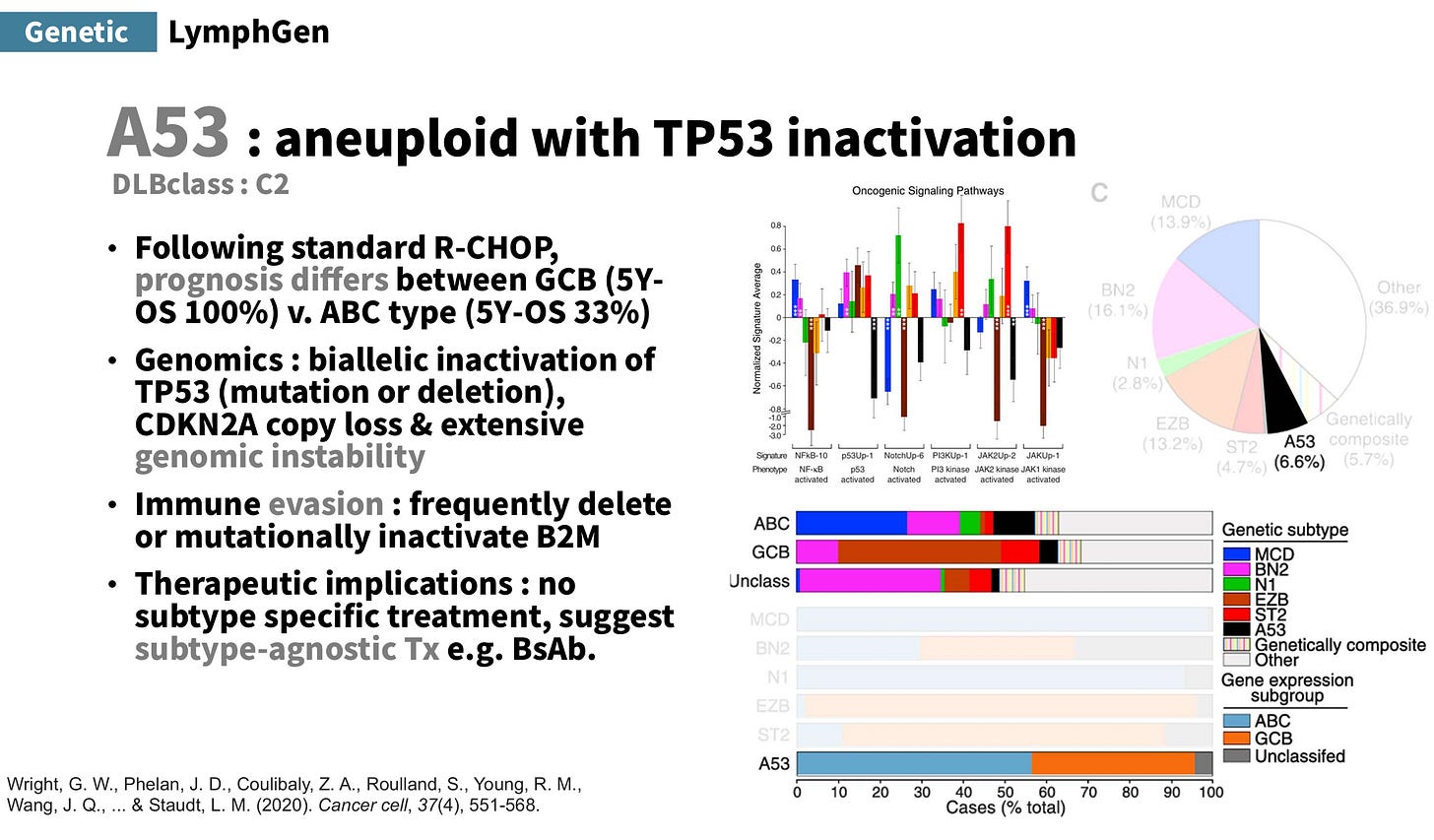
A53 型/DLBclass-C2:代表基因特徵為非整倍體(aneuploid)合併 TP53 inactivation。接受標準 R-CHOP 後,預後依細胞來源不同而差異很大,GCB 的 5 年 OS 100%,而 ABC 5 年 只有 OS 33%。具有廣泛基因不穩定性,而且有免疫逃脫(常見 B2M 缺失)。目前沒有明確針對此分型的治療,較傾向考慮 subtype-agnostic 治療,例如 bispecific antibodies (BsAb)
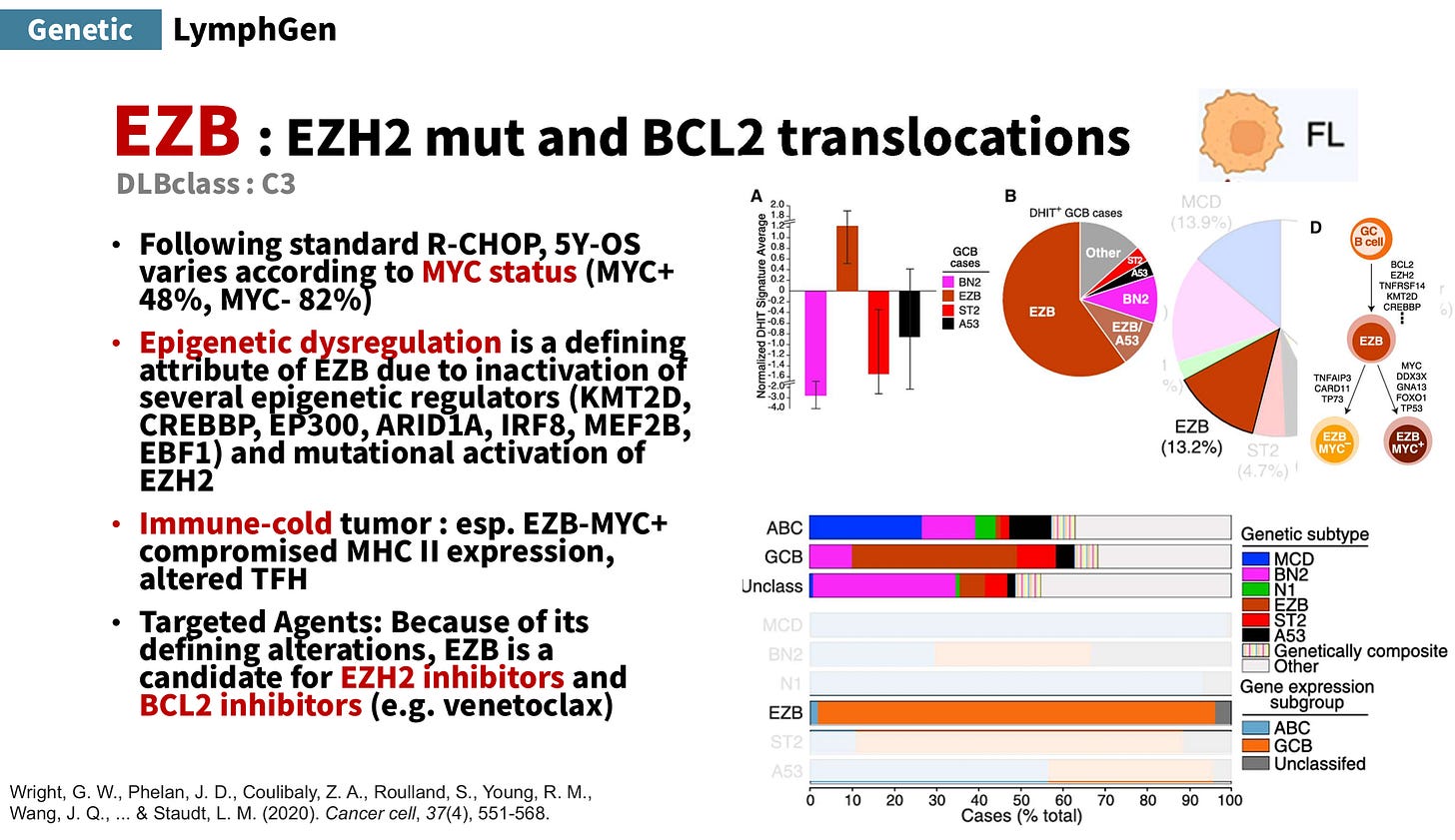
EZB 型/DLBclass-C3:代表基因特徵為 EZH2 突變 與 BCL2 translocation,接受標準 R-CHOP 後,預後受 MYC 狀態影響很大。MYC+:5 年 OS 約 48%,而 MYC−:5 年 OS 約 82%。該型以表觀遺傳失調(epigenetic dysregulation)為重要特徵
涉及 KMT2D, CREBBP, EP300, ARID1A, IRF8, MEF2B, EBF1 等調控因子功能異常,以及 EZH2 活化。免疫上屬於 immune-cold tumor,特別是 EZB-MYC+,可見 MHC II 表現受損。因其分子特徵,適合考慮 EZH2 inhibitors 與 BCL2 inhibitors(如 venetoclax)。
以上便是基因分型流變與細項的介紹,下一篇在講因應分型的治療與臨床試驗。