前面兩章分別簡述了 DLBCL 的分型系統以及細項。
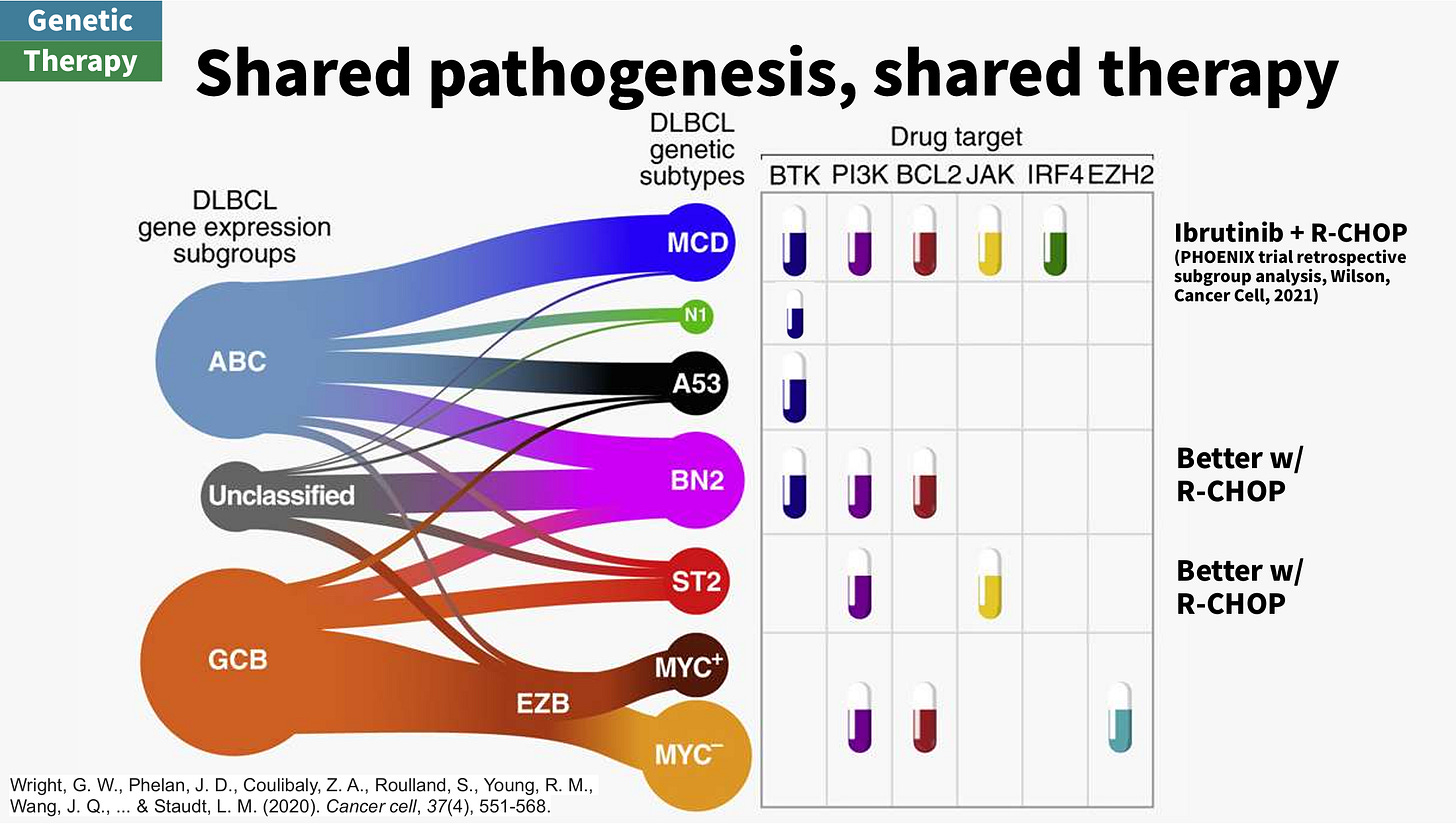
接下來則會介紹基因不同分型下對應的治療。可以先參考提出 LymphGen 的 Wright 等人建議的治療選項。
新藥物或新組合的分群分析
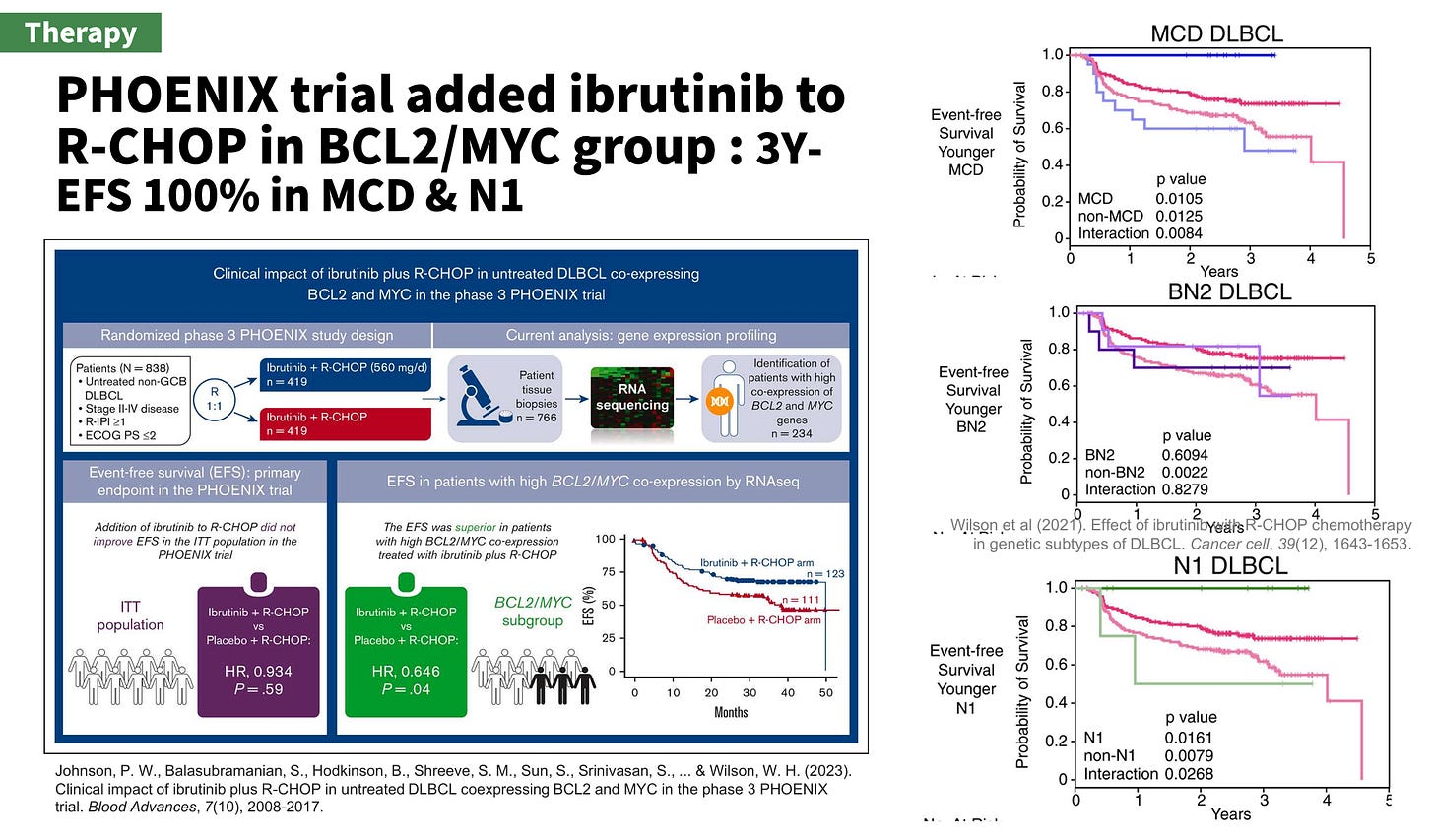
PHOENIX trial : 將 ibrutinib 加入 R-CHOP 作為 DLBCL 第一線治療的三期試驗,而在BCL2/MYC 組內 3Y-EFS 100% in MCD & N112。BN2 效果也還不錯,但就沒有像 MCD, N1 那麼好。
POLARIX trial : Pola-R-CHP 對於 non-GCB 的效果很好,可以在一線治療就將 non-GCB type 與 GCB 拉齊,而在復發後使用的話在 non-GCB 效果更好,在事後分析(post-hoc analysis)發現 EZB 與 MCD 組似乎有較佳的 2Y-PFS 趨勢,而 BN2 使用 Pola-R-CHP 的話兩年疾病無惡化存活期(Progression free survival, PFS)較差3。更棒的消息時,用 IHC 來區分 COO 在 polatuzumab 的使用效果上,non-GCB 是個很強的預測因子4。這樣就毋須動用很貴的基因表現陣列(Gene expression profile, GEP)。
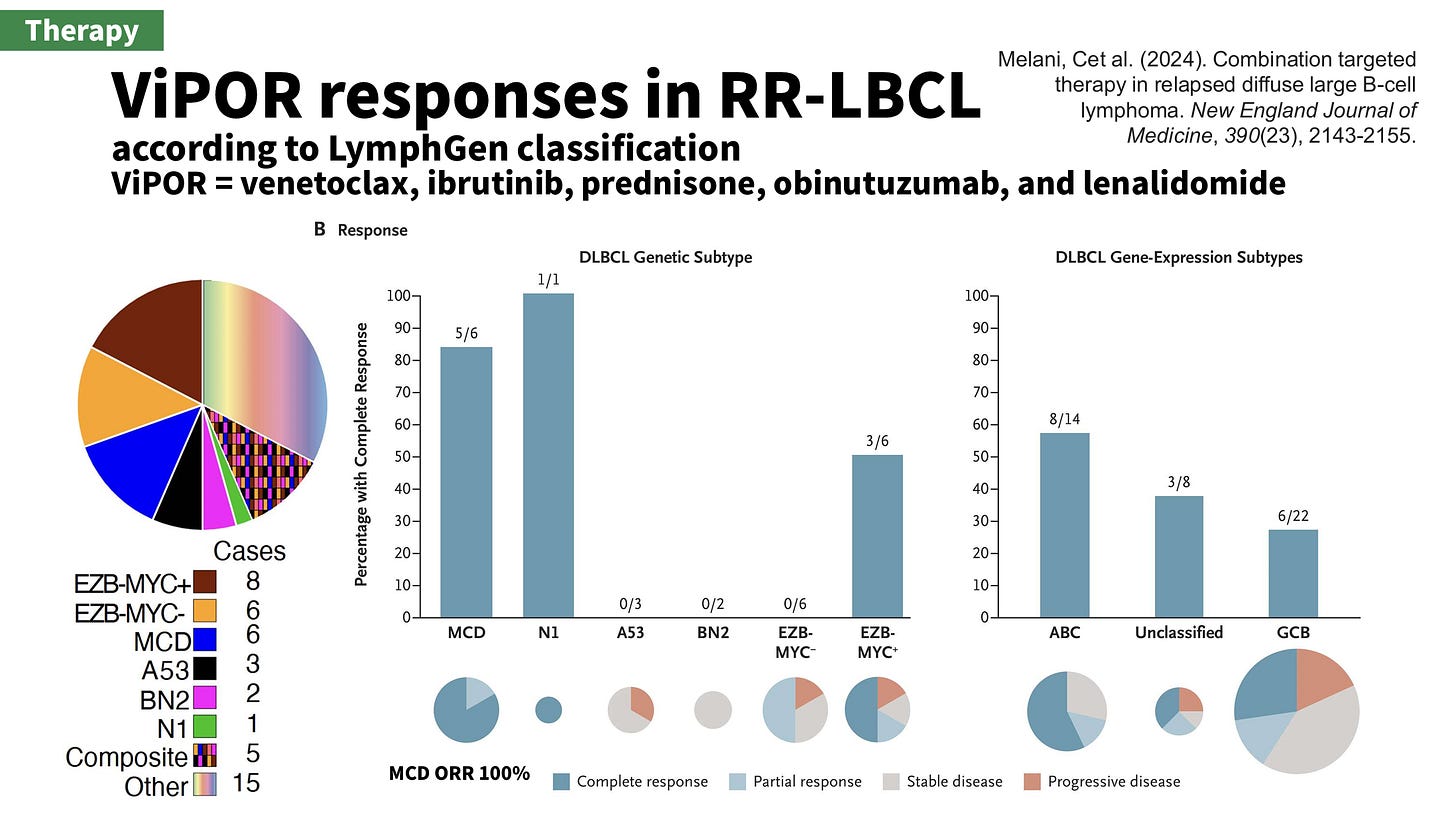
NCT03223610 : 登上 NEJM 的著名組合 ViPOR(venetoclax, ibrutinib, prednisone, obinutuzumab, and lenalidomide)5,在 MCD 與 N1 組的整體反應率(Overall response rate, ORR)達 100%,在 EZB-MYC+ 組也很不錯。可惜這個試驗的人數少,這個組合也極其昂貴。
針對基因分型設計的試驗
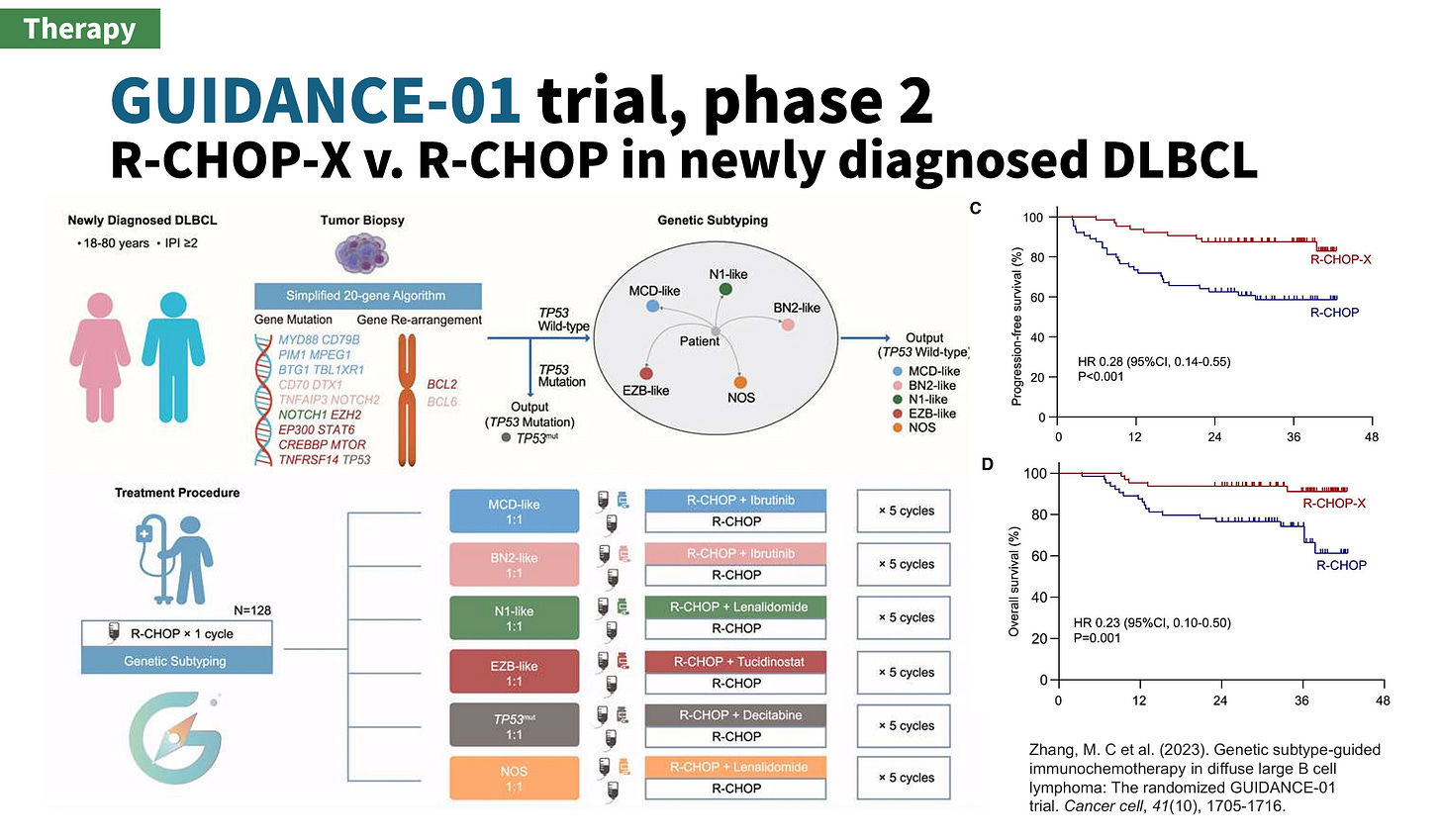
最著名的針對 DLBCL 基因分型的傘型試驗(umbrella trial)莫過於 GUIDANCE-01 trial6。R-CHOP-X 對上 R-CHOP 讓實驗組的 PFS 與總存活率(Overall survival, OS)的風險比(Hazard Ratio, HR)可以到 0.23-0.28,而且具統計意義。
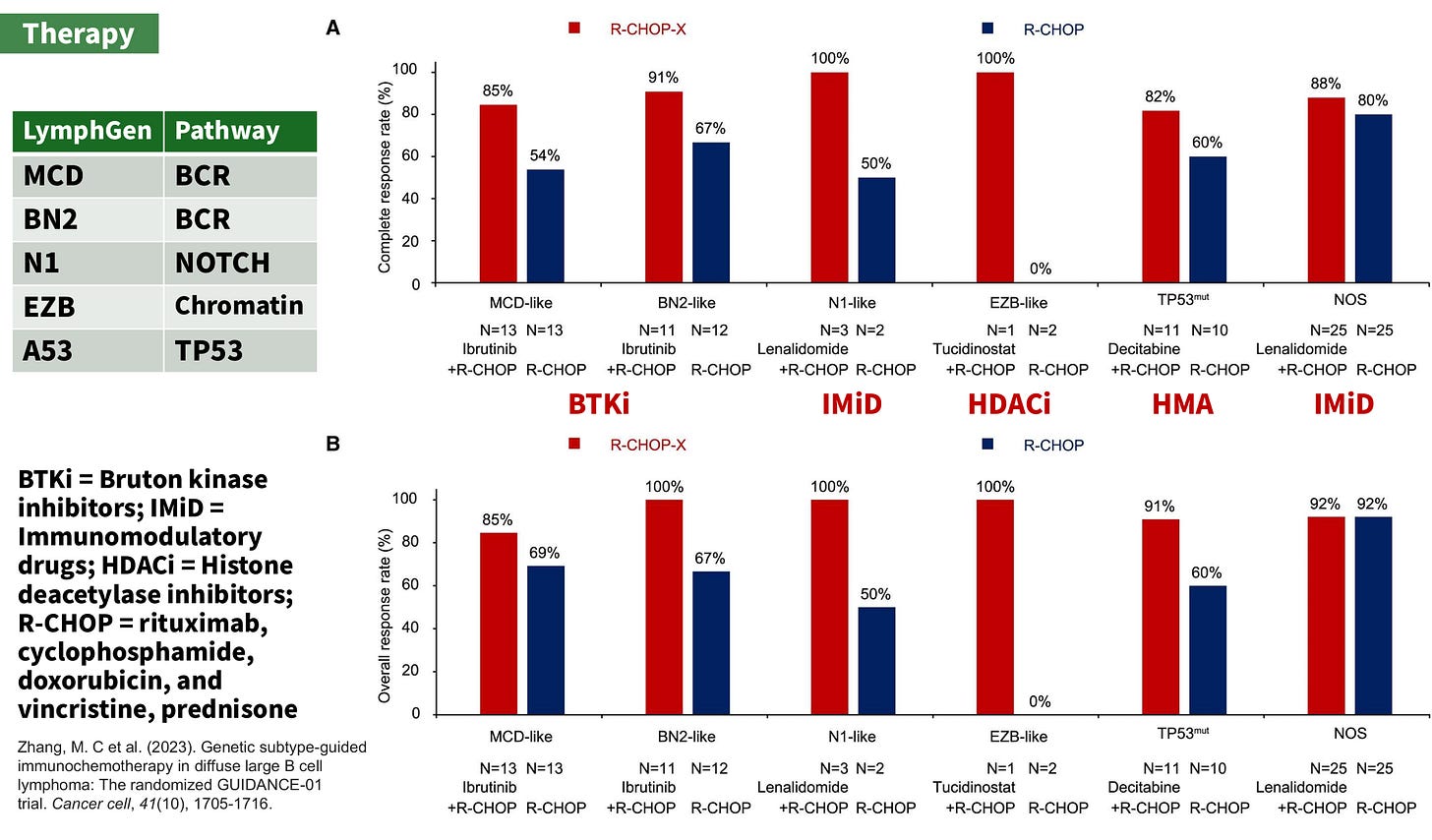
它的設計是 MCD-like, BN2-like 加上 BTK inhibitor, Ibritinib,而 N1-like 與無法分型者加上 Lenalidomide,EZB 加上 Tucidonostat,一種亞型選擇性組蛋白去乙醯化酶抑制劑(Histone deacetylase inhibitor, HDACi),而 TP53 突變者,亦即 A53-like,則加上 Decitabine。
可以從各別反應的圖看到只要有個分型的對應治療,反應都很好,而 NOS 則是 Lenalidomide 有加或沒加都一樣。
在 GUIDANCE-01 這個第二階試驗大獲成功後,便接著第三階 GUIDANCE-02。而 GUIDANCE-05 則是將 R-CHOP 換成了 Pola-R-CHP,GUIDANCE-06 則是針對復發或難治型的病人。
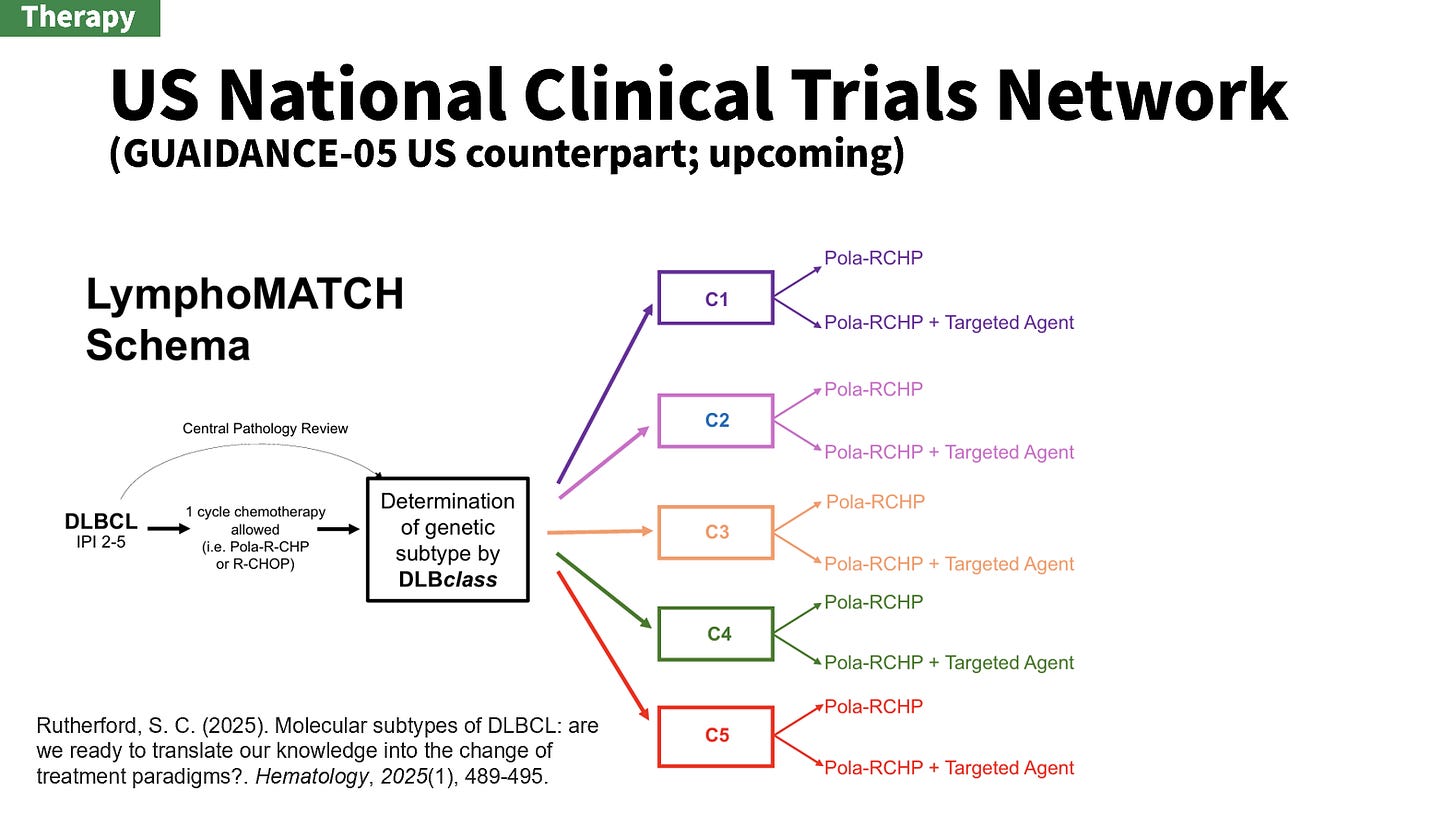
美國則不干示弱,設計了 LymphoMATCH 試驗7,和 GUIDANCE-05 一樣以 Pola-R-CHP + X 為一線,只是用的不是 LymphGen 分法,而是 DLBclass。
總結
最廣為使用的 DLBCL, NOS 分型成是以 IHC 來區分 COO。它便宜好用,即使可能導致 15-50% 的錯誤分類,仍是個標靶化藥 Polatuzumab 的效果預測方式。
暗區標記(Dark zone signature)可以抓出 FISH 陰性的 double hit lymphomas。這群病人預後極差。
DLBCL 基因分類以這兩個系統 LymphGen & DLBclass 為主。提供我們更多關於病生理機轉、預後,甚至藥物選用的參考。
因著基因分類的試驗更如火如荼的進行當中,包括 GUIDANCE, LymphoMATCH。期待後續更新。
如果雙標靶藥物被提到了 DLBCL 的一線,或許整個基因分類又要被改寫了。
Johnson, P. W., Balasubramanian, S., Hodkinson, B., Shreeve, S. M., Sun, S., Srinivasan, S., ... & Wilson, W. H. (2023). Clinical impact of ibrutinib plus R-CHOP in untreated DLBCL coexpressing BCL2 and MYC in the phase 3 PHOENIX trial. Blood Advances, 7(10), 2008-2017.
Wilson et al (2021). Effect of ibrutinib with R-CHOP chemotherapy in genetic subtypes of DLBCL. Cancer cell, 39(12), 1643-1653.
Tilly, H., et al (2022). Polatuzumab vedotin in previously untreated diffuse large B-cell lymphoma. New England Journal of Medicine, 386(4), 351-363.
Cliff, et al (2026). Cell-of-Origin Subtype Predicts Response to Polatuzumab Vedotin in Large B-cell Lymphoma. Clinical Cancer Research, 32(1), 159-168.
Melani, Cet al. (2024). Combination targeted therapy in relapsed diffuse large B-cell lymphoma. New England Journal of Medicine, 390(23), 2143-2155.
Zhang, M. C et al. (2023). Genetic subtype-guided immunochemotherapy in diffuse large B cell lymphoma: The randomized GUIDANCE-01 trial. Cancer cell, 41(10), 1705-1716.
Rutherford, S. C. (2025). Molecular subtypes of DLBCL: are we ready to translate our knowledge into the change of treatment paradigms?. Hematology, 2025(1), 489-495.